ARTÍCULO DE REVISIÓN
REVISTA DE LA FACULTAD DE MEDICINA HUMANA 2021 - Universidad Ricardo PalmaDOI 10.25176/RFMH.v21i3.4016
ABORDAJE DE CONTROL DE DAÑOS Y REANIMACIÓN REDUCIDA DEL PACIENTE PEDIÁTRICO POLITRAUMATIZADO EN URGENCIAS.
DAMAGE CONTROL APPROACH AND REDUCED RESUSCITATION OF THE POLYTRAUMATIZED PEDIATRIC PATIENT IN THE EMERGENCY ROOM.
Augusto Flavio Figueroa-Uribe(1,a), Julia Hernández-Ramírez(1,b), Gabriela Mendoza-Besares(1,c), Inti Ernesto Bocanegra-Cedillo(2,d), Michelle Fabienne Vela-Díaz(1,e), Jorge Omar Flores-del Razo(1,f)
1 Hospital Pediátrico Peralvillo SSCDMX, Ciudad de México México
2 Hospital de Traumatología y Ortopedia, IMSS, Monterrey, N.L, México
a Urgenciólogo Pediatra, Subdirector Médico
b Enfermera Pediatra, Coordinadora de Enseñanza
c Urgencióloga Pediatra, Jefe de Urgencias
d Intensivista Pediatra, Médico Adscrito a la UMAE No. 21
e Urgencióloga, Médico adscrito al Servicio de Urgencias
f Urgenciólogo Pediatra, asistente de la Dirección
El politrauma en el paciente pediátrico es un evento frecuente por lo que su abordaje y manejo oportuno definen el pronóstico del mismo. Se define como politrauma a la presencia de dos o más lesiones traumáticas o una sola que pone en peligro la vida o existe el riesgo de secuelas graves; la reanimación se entiende como el restablecimiento de las funciones vitales del paciente en el área prehospitalaria hasta el área hospitalaria encaminados a evitar el daño causado por la pentada mortal del trauma (coagulopatía, acidosis, hipotermia, hiperglicemia e hipoxia) por lo que se realizó el protocolo de control de daños el cual es referido a todas la maniobras que tiene el fin de preservar la vida, pero sin llevar a cabo reparaciones definitivas con el objetivo de mitigar complicaciones derivadas del estado de choque prolongado, secundario a un tiempo quirúrgico prolongado que postergaba la reanimación adecuada, ésta reanimación reducida consta de 6 indicaciones precisas para su realización, siendo abordado desde el TEP (Triangulo de evaluación pediátrica) y protocolo MARCHDEF (Hemorragias masivas, Vía aérea, Respiración, Circulación, Hipotermia, Déficit Neurológico, Glicemia, Dolor, Exposición, FAST).
Palabras Claves: Politrauma, Control de daños, Reanimación reducida, TEP, MARCHDEF. (Fuente: DeCS - BIREME)
ABSTRACT
Polytrauma in pediatric patients is a frequent event, so its timely approach and management define its prognosis. Polytrauma is defined as the presence of two or more traumatic injuries or a single one that endangers life or there is a risk of serious sequelae; resuscitation is understood as the restoration of vital functions of the patient in the pre-hospital area to the hospital area aimed at avoiding the damage caused by the fatal pentad of trauma (coagulopathy, acidosis, hypothermia, hyperglycemia and hypoxia) for which the Damage control protocol which is referred to all the maneuvers that have the purpose of preserving life, but without carrying out definitive repairs in order to mitigate complications derived from the prolonged state of shock, secondary to a prolonged surgical time that postponed adequate resuscitation, this reduced resuscitation consists of 6 precise indications for its performance, being approached from the TEP (Pediatric Evaluation Triangle) and the MARCHDEF protocol (Massive Bleeding, Airway, Breathing, Circulation, Hypothermia, Neurological Deficit, Glycemia, Pain, Exposure, FAST).
Keywords: Politrauma, Damage control, Reduced resuscitation, TEP, MARCHDEF. (Source: MeSH – NLM)
Cuando un paciente tiene dos o más lesiones traumáticas o sólo una que pone en peligro su vida o presenta riesgo de padecer una secuela grave definimos el concepto de politraumatismo; el traumatismo cráneoencefálico es el más frecuente y muchas veces está asociado a lesiones en otras partes de cuerpo.
La muerte en el paciente pediátrico con politraumatismo generalmente se presenta en los primeros minutos después de un accidente y las causas reportadas como más frecuentes son las lesiones en el cerebro, médula y grandes vasos; sólo la tercera parte de las muertes (30%) acontecen en las horas posteriores al accidente por hipovolemia, hemorragia o hipoxia.
Reanimación abreviada
La reanimación es el restablecimiento de las funciones vitales del niño, en este caso, víctima de trauma, que inicia en la atención prehospitalaria para continuar en la atención hospitalaria con los procedimientos invasivos necesarios para disminuir y evitar el daño causado por coagulopatía, acidosis, hipotermia, hiperglicemia e hipoxia(1).
Este concepto se empezó a aplicar durante la guerra de Vietnam en donde se observaban lesiones por trauma que provocaban coagulopatía y acidosis, por lo que se propuso la hemotransfusión temprana con sangre reconstituida. Durante la guerra de Afganistán, en la primera década del siglo XXI, se sistematizó la forma de manejo de los pacientes con trauma de alta energía y se aplicó el pensamiento de reanimación de control de daños o reanimación abreviada(1).
En la década de 1970, la Universidad de Pensilvania propuso el protocolo de control de daños que incluía la forma de manejo del paciente con trauma de alta energía, fracturas múltiples y estado de shock exanguinante; referido a todas las maniobras que tienen el fin de preservar la vida del paciente, pero sin llevar a cabo reparaciones definitivas, ya que toman tiempo y perpetuán el estado de shock e hipotermia del paciente. Los pacientes fallecían más por complicaciones derivadas del estado de shock prolongado, secundario a un tiempo quirúrgico también prolongado que postergaba la reanimación óptima del paciente.
Las indicaciones de reanimación con control de daños son seis:
- Gravedad de las lesiones, definida por la presencia de dos lesiones u órganos o sistemas que ponen en peligro la vida del paciente; la mayoría de veces son secundarias a trauma de alta energía o tienen índice de gravedad de daño mayor a 35 puntos.
- Estado de shock exanguinante con pérdida de 28% o más del volumen circulante del paciente pediátrico (80 a 90cc kg) por más de 70 minutos, que se puede complicar con coagulopatía de consumo.
- Invertir tiempo en procedimientos que no mejorarán la sobrevida del paciente o la insuficiente experiencia del médico en la realización del mismo.
- Hipotermia menor a 34°, acidosis con pH <7,2 y coagulopatía (tiempo de protrombina >19seg, tiempo de tromboplastina parcial <60 o >60 seg, lactato sérico > 5 mmo/l y déficit de base > 6mmol/L).
- Incapacidad para bloquear hemorragias externas o internas (intrabdominal o torácica).
- Presencia de comorbilidades asociadas como diabetes, obesidad, cardiopatía, enfermedad renal, malformaciones, edad menor de 5 años o mayor de 60 años(1).
El modelo recomendado para la evaluación consta de una evaluación general e inicial del niño mediante el triángulo de evaluación pediátrica (TEP) y las evaluaciones primaria, secundaria y terciaria. El fin es reconocer signos de disfunción del sistema nervioso central, dificultad respiratoria, insuficiencia respiratoria, shock compensado y shock descompensado para poder intervenir oportunamente y salvar la vida del paciente. Si los pacientes no se tratan oportunamente pueden progresar rápidamente a insuficiencia cardiopulmonar cuyo desenlace final es el paro cardiaco(2).
El esquema básico de atención es el siguiente:
- Evaluación general
- Evaluación primaria (Sistema MARCHDF)
- M. Hemorragias masivas
- Vía aérea
- R. Respiración
- C. Circulación
- H. Hipotermia
- D. Déficit neurológico/Glicemia capilar (Destrotix®)/Discapacidad neurológica (Glasgow), Dolor
- E. Exposición
- Fármacos, FAST, Familia.
- Evaluación Secundaria. (Sistema MESIRT)
- Monitorización
- Exploración cráneocaudal
- SAMPLE Historia clínica simplificada
- Interconsultas
- Revaloración
- Traslado
Utilice el modelo “evaluar-identifico-intervengo” para evaluar y tratar al paciente pediátrico que se encuentra herido y grave. Realice una evaluación inicial y proceda a repetir la evaluación con la finalidad de decidir el mejor tratamiento o intervención para el paciente. Categorice el estado clínico según el tipo y gravedad, decida y actúe para iniciar el tratamiento. Posteriormente, revalúe y repita el proceso “evaluar-identifico-intervengo”.
Si se identifica un inconveniente potencialmente mortal, proceda a iniciar las intervenciones necesarias para salvar la vida del niño y utilice la evaluación con enfoque sistemático(1,2,3,4,5).
Triangulo de evaluación pediátrica TEP
El TEP es un enfoque para la evaluación inicial, especialmente adaptado para niños. Es una herramienta rápida, sencilla y útil para evaluar a niños de todas las edades; permite integrar características del paciente con las que se forma la impresión general independientemente de la enfermedad o lesión. El TEP se ha convertido en el modelo básico de evaluación en los programas nacionales e internacionales de apoyo vital(1). Es un instrumento sencillo para empezar la evaluación de un niño exclusivamente sobre la base de indicios visuales y auditivos, no requiere de estetoscopio, esfigmomanómetro, monitor cardiaco, ni de oxímetro de pulso. Utilice la herramienta del TEP en el lugar donde se hace el primer contacto con el paciente, la evaluación debe realizarse en 30 a 90 segundos.
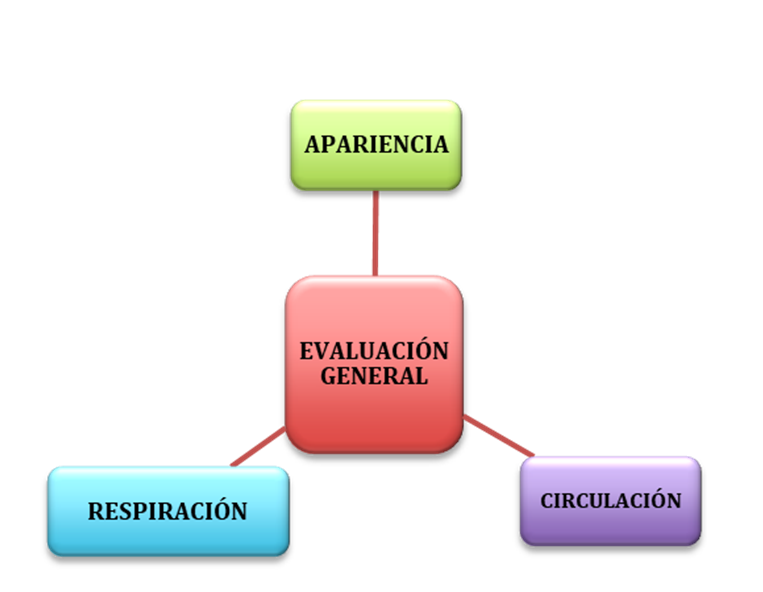
En realidad, el TEP es el paradigma de evaluación a primera vista. Los tres componentes del TEP reflejan el estado fisiológico general de oxigenación, ventilación, perfusión y función cerebral. Los componentes del TEP son la apariencia (conciencia o inconciencia, irritabilidad, hiperreactividad, hiporreactividad y sangrados) circulación (cianosis, palidez y piel marmórea) y respiratorio (apnea, disnea, polipnea o bradipnea) y respiración (ruidos anormales y signos de trabajo respiratorio). El TEP es una herramienta más no un instrumento que facilita al personal de la salud de primer contacto a otorgar el apoyo vital al paciente en situación de emergencia.
Los tres componentes del TEP (Figura1) permiten la evaluación inicial del estado cardiopulmonar, función cerebral y metabolismo del niño, así como la identificación del tipo y la gravedad del estado fisiológico para iniciar lo más pronto el tratamiento(1,2,6).
Figura 1. Concepto de evaluación general o TEP: a. Apariencia: Alteración de la conciencia o sangrados; b. b. Circulación: Coloración, cianosis, palidez, marmóreo, etc.; c. Respiratorio: Aumento o disminución del trabajo respiratorio o sonidos anormales como estridor o quejido respiratorio
- Si el paciente presenta dificultad respiratoria, se lo coloca en una posición cómoda y se le administra oxigeno suplementario según lo requiera, además se empieza la terapia específica para las posibles etiologías. Si el paciente presenta insuficiencia respiratoria, se revisa la posición de la cabeza, la permeabilidad de la vía aérea y se administra oxígeno al 100 % mediante ventilación bolsa-mascarilla según sea necesario. En el caso de presentar cuerpos extraños se procede a la extracción de los mismos. Por último, se obtiene una vía aérea avanzada.
- En el caso del paciente con shock se administra oxígeno.
- En una situación de riesgo vital es importante verificar la adecuada posición de la cabeza, mantener la vida aérea permeable y si es necesario se procede a la intubación orotraqueal, se inicia ventilación con el dispositivo correspondiente, se administra oxígeno al 100% y se inician maniobras de reanimación.
El TEP por lo fácil y práctico de realizar y recordar, asegura que todo el personal de salud involucrado en los servicios de urgencias “hable el mismo idioma”, permitiendo categorizar rápidamente la alteración que presenta el paciente pediátrico. Constituye el primer peldaño para priorizar la atención del paciente grave que acude a los servicios de urgencias tan sólo respondiendo a las siguientes preguntas:
- ¿Qué tan grave es la lesión del paciente pediátrico?
- ¿Cuál es la probable anormalidad fisiológica?
- ¿Cuál es la urgencia de la atención para iniciar el tratamiento?
Los tres componentes son esenciales para mejorar la eficiencia y eficacia de la atención, ambos indicadores de calidad en los servicios de urgencias(7).
Evaluación primaria
La evaluación primaria es una evaluación clínica que consiste en una exploración rápida y sistemática con la finalidad de detectar lesiones que constituyen un riesgo vital para el paciente; el tratamiento debe ser eficaz y sencillo.
Sistema MARCH-DEF
Acrónimo utilizado y aceptado por el comité de trauma de los Estados Unidos para el manejo y abordaje de los diez minutos de platino en el paciente pediátrico y en el adulto politraumatizado en un ambiente pre hospitalario y hospitalario convencional y hostil(1,7,8).
M Massive hemorrage (Hemorragia masiva)
La primera causa de muerte dentro de la primera hora de la atención de trauma es el sangrado exanguinante que provoca en poco tiempo choque hemorrágico, acidosis y coagulopatía por consumo. El control rápido, eficaz y eficiente de las hemorragias exanguinantes con agentes compresivos (torniquetes, vendajes compresivos, gasas hemostáticas, etc.) y agentes hemostáticos según protocolo, estado de la víctima y situación del lugar, es prioridad en la atención del paciente politraumatizado. Una hemorragia que comprometa un vaso principal, arteria o vena, puede provocar la muerte entre cinco a diez minutos. Por lo tanto, el manejo de la hemorragia es prioridad máxima(9,10)
Agentes hemostásicos sistémicos
El ácido tranexámico (ATX) es un derivado sintético del aminoácido lisina e inhibe la fibrinólisis mediante el bloqueo de los sitios de fijación de la lisina en el plasminógeno, el cual puede administrarse en una amplia gama de patologías en el entorno de la atención médica.
Los niños cuentan con un reducido volumen sanguíneo en comparación con los adultos y no pueden tolerar grandes pérdidas de volumen de sangre; sin embargo la falta de enfermedades cardíacas y vasculares en ellos permite una mayor capacidad de compensación durante el shock hemorrágico(10).
La incidencia del uso de ATX en trauma pediátrico es baja; no obstante, consideramos que su incorporación en el manejo de trauma pediátrico tiene el potencial de reducir significativamente la mortalidad en niños y jóvenes sin aumentar los eventos adversos, por lo que se sugiere considerar su uso.
Se recomienda su aplicación de manera temprana siguiendo el protocolo usado en adultos; dosis de carga de 1 g aplicado en el lapso de 10 minutos dentro de las primeras 3 horas después de la lesión, seguido de una infusión de 1 g durante 8 horas para los niños con edad mayor a 12 años. Para los menores de 12 años de edad, la dosis de carga es 15 mg / kg (dosis máxima 1 g) se continua de una infusión de 2 mg / kg / hora durante al menos 8 horas o hasta que cesa el sangrado. Los efectos adversos de TXA en pediatría son muy raros, sin embargo bajo el contexto de trauma reconocemos que son necesarias más investigaciones; debido a que algunos estudios cuentan con niveles y grados de recomendación muy bajas(3,11).
La primera medida de atención es la compresión directa con gasa hemostática o vendaje compresivo tipo israelí(10,11). (Figura 2).
Torniquetes
Se han publicado pocos estudios relacionados a la experiencia prehospitalaria con torniquetes en niños. La Sociedad de Trauma Pediátrico, apoya el uso de torniquetes en ámbito prehospitalario y durante la reanimación en aquellos pacientes que sufren de hemorragias exanguinantes (grado de recomendación C/D)*.
Hay que recordar que durante el atentado de Boston muchas de las víctimas eran niños y los primeros respondientes colocaron torniquetes a varias víctimas pediátricas con hemorragias exanguinantes que salvaron la vida con esta intervención sencilla. En el año 2012, aparece la guía pediátrica de TECC (Tactical Emergency Casualty Care) en la cual se permite su utilización en el paciente pediátrico.
Los niños víctimas de violencia presentan generalmente patrones de lesión similares a los adultos; por lo tanto en ellos también puede estar indicado el uso de torniquetes con la finalidad de lograr el control de las hemorragias en los miembros. Después del atentado de Boston la Academia Americana de Pediatría recomienda la utilización en niños del torniquete tipo STAT.
Con la finalidad de obtener la máxima seguridad y utilidad clínica en los pacientes pediátricos de los diferentes grupos de edad, es necesario realizar investigaciones en el ámbito pediátrico para evaluar el tamaño de los torniquetes considerando las características fisiológicas de los niños y otros aspectos relacionados con este tipo de pacientes(12).
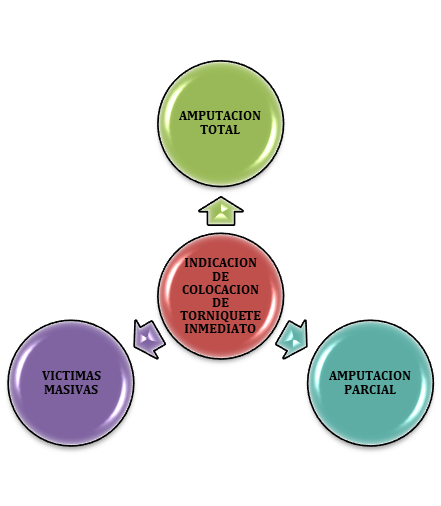
Indicaciones clínicas absolutas de colocación inmediata de torniquete en pediatría(Figura 3).
- En amputaciones de magnitud importante con presencia de hemorragia externa moderada o severa.
- Sangrado importante no controlable por compresión directa o vendaje hemostático.
- Sangrados múltiples en diferentes focos que no permiten la aplicación óptima de presión directa.
- Pacientes con hemorragias externas graves en miembros que requieren urgente de soporte ventilatorio o de aislamiento de la vía aérea.
- Hemorragia no controlada generada por objeto penetrante(1,4).
La mejor táctica para controlar el sangrado dependerá de una serie de factores tales como el estado de la víctima, la magnitud y gravedad de la hemorragia, la proximidad a un establecimiento de salud con capacidad resolutiva quirúrgica, el número simultáneo de heridos, la accesibilidad de recursos humanos y de medios de transporte, así como del adiestramiento del personal de salud de la unidad de shock de urgencias en materia de control de daños, pues son ellos quienes brindaran la primera asistencia en un hospital(12).
Airway (Vía aérea)
El paciente politraumatizado siempre se debe considerar como “vía área difícil”. En estos pacientes es obligatorio administrar oxigeno suplementario para mantener la oxigenación y prevenir la hipoxemia.
La obstrucción de la vía aérea es la principal causa de mortalidad evitable en el politraumatismo. Es producida en pacientes inconscientes por la caída de la lengua hacia la faringe y en pacientes conscientes por la obstrucción de la vía aérea con sangre, vómito, edema, cuerpos extraños o restos alimenticios(13).
La primera fase del reconocimiento se caracteriza por tres alertas:
- Alerta cervical
- Alerta del estado de conciencia
- Alerta de la vía aérea
Se refiere a la inmediata estabilización cervical para lo cual el ayudante mantendrá la cabeza-cuello-tronco alineados e inmovilizados en una posición neutra. Se procederá a colocar el collarín sólo si la actual situación del paciente no requiere de intubación.
- Si fuese necesario el manejo instrumental de la vía aérea se procede con la inmovilización bimanual y una vez que la vía aérea se encuentra establecida se colocará el collarín.
- Es fundamental recordar que la restricción selectiva de movimientos espinales es lo que ha probado mejores resultados en niños (NICE 2016).
- Siempre se deberá retirar el collarín para revisar el cuello
Consiste en determinar el estado de alerta del niño; como norma general todo paciente consciente que habla o respira tiene la vía aérea permeable. Si el paciente estuviese inconsciente, con presencia de ruidos respiratorios anormales, respiración irregular o tirajes se inicia inmediatamente al manejo instrumental de la vía aérea(13).
Alerta de la vía aérea
En el escenario que la vía aérea se obstruya se procede a su desobstrucción mediante la aspiración de secreciones o remoción de cuerpos extraños. Para mantener la vía aérea permeable se utiliza cánulas orofaríngeas; tener presente que el paciente semiinconsciente o consciente puede presentar vómitos o laringoespasmo con riesgo de broncoaspiración. Si no se aprecia mejoría, la intubación orotraqueal es lo indicado, con lo que se logra el control definitivo de la vía aérea, recordar que tiene indicación en las diferentes fases de la evaluación inicial del paciente pediátrico politraumatizado. Recordar emplear una secuencia rápida de intubación con premedicación. La intubación debe realizarse retirando el collarín, inmovilizando la columna cervical de manera bimanual y utilizando siempre una guía tipo bougie. Otras opciones de manejo avanzado de vía aérea, en caso de no lograr intubación orotraqueal, incluyen dispositivos supraglóticos, de preferencia aquellos que coadyuven posteriormente a la intubación orotraqueal (dispositivo SALT, LMA fastrack, tubos laríngeos) así como la cricotomía en casos extremos(14,15).
R. Respiración
Asegure la vía área y proceda a inmovilizar el cuello. Luego evalúe la función pulmonar del paciente (oxígeno y ventilación) y detecte signos de insuficiencia respiratoria grave. Evalúe la posición de los órganos para detectar la presencia de cianosis, congestión del cuello, dilatación del tórax, disnea y calidad del aire pulmonar. Si se presentan síntomas de insuficiencia respiratoria persistente, es importante descartar la presencia de un neumotórax a tensión antes de intubar(16). En esta etapa, es fundamental detectar lesiones torácicas fatales como neumotórax a tensión, neumotórax abierto y neumotórax masivo. Debido a la rápida progresión, el diagnóstico debe basarse en la evidencia clínica, sin esperar la confirmación radiológica para el tratamiento. Cuanto mayor es el paciente y menor la complexión es menos resistente al neumotórax. El ventilador puede convertir un neumotórax simple en un neumotórax a tensión, y siempre que se sospeche neumotórax a tensión durante el tratamiento hospitalario se debe priorizar el drenaje sobre la punción (NICE 2016); si esto no se puede lograr y / o si la condición no está permitida, se debe realizar inmediatamente una toracocentesis en el segundo espacio intercostal, línea medio clavicular, con catéter 14 o 16 G acoplado a un sello de agua o válvula de Helmich que cumple la misma función. En el caso de neumotórax abierto, la conducta es sellarlo para evitar un neumotórax a tensión y convertirlo en un neumotórax simple que se controla como se describió anteriormente. El hemotórax masivo corresponde a la presencia de sangre en la cavidad pleural causando inestabilidad hemodinámica (> 20 cc / kg / hr o> 25% del volumen sanguíneo en pacientes pediátricos). El tratamiento consiste en colocar un tubo de drenaje torácico en el quinto espacio intercostal a nivel de la línea axilar media y realizar una potente reposición de volumen(15).
C. Circulación. Manejo hemodinámico de control de daños
Después de asegurarse de que la vía aérea no esté obstruida y de verificar la oxigenación y ventilación, debe evaluar el estado circulatorio del paciente: Primero, confirme el lugar donde previamente se colocó el dispositivo de compresión, pues la gasa hemostática previene el sangrado; si el sangrado continúa, debe evaluar la colocación de un segundo torniquete. Si se usa el primero o el dispositivo de tela para la compresión, el primer torniquete debe ser colocado. Si el paciente está amputado, el torniquete se aplica de inmediato(16,17).
Posteriormente, el paciente debe ser evaluado clínicamente para detectar signos de shock hipovolémico y clasifique su gravedad (compensado o descompensado/hipotenso). Analice lo siguiente para determinar la gravedad:
- Pulsos centrales y periféricos
- Llenado capilar (<4 segundos)
- Temperatura
- Frecuencia cardiaca
- Tensión arterial
Al canalizar la vía venosa, ya sea por vía intravenosa o intraósea, se debe recolectar muestra de sangre para hemograma completo, pruebas cruzadas para transfusión y glicemia, esta última utilizando destroxtix, para descartar hiperglucemia o hipoglucemia.
El estándar de oro para tratar el shock traumático por hipovolemia causado por hemorragia es administrar de inmediato sangre reconstituida (NICE 2016). Se debe valorar la posibilidad de aplicar protocolos de transfusión masiva balanceada con la clasificación ABC de transfusión masiva. Si aparecen signos de shock administrar líquidos para mejorar la hemodinámica(19). Se debe manejar reposición de líquidos restrictiva, es decir de no contar con sangre utilizar como segunda opción solución salina hipertónica al 3% a una dosis de 5-10 cc kg en 20 minutos para evitar el fenómeno de reperfusión y la inestabilidad de los coágulos ya formados (Fenómeno" popping the Clot"), tres dosis, de no poder aplicar esta opción utilizar solución salina al 0,9% a la dosis de 20 cc kg durante 20 minutos(20).
Si la hemorragia no se ha controlado iniciar manejo de hipotensión permisiva y reanimación retardada con solución salina hipertónica al 3% de 5 a 10 cc/ kg en 20 minutos con la finalidad de evitar complicaciones como coagulopatía de consumo, síndrome de reperfusión y síndrome de compartimental interno. La medida de hipotensión permisiva está contraindicada cuando el paciente presenta traumatismo craneoencefálico y en menores de 5 años(17). En pacientes de 5 a 17 años de edad con una lesión en la cabeza se prohíbe las medidas permisivas de hipotensión(17). Cuando finalice cada bolo de la solución, revise la respuesta hemodinámica del paciente explorando nuevamente los datos clínicos cardiovasculares, así como los signos de fuga a tercer espacio (pulmón). Si ya no presenta signos de shock, se infunden líquidos a necesidad basal. Seguramente el paciente perdió menos del 20% del volumen circulante. Si no responde se debe valorar la administración de un nuevo bolo de corticoide y/o trasfusión de sangre total si la tuviera.
Se debe buscar sangrados aún no controlados o sangrado oculto. En los recién nacidos y lactantes menores de 8 kilos el sangrado intracraneal por si solo puede provocar datos de shock hipovolémico severo además de compromiso neurológico concomitante(7,20).
H. Hipotermia
En mayores de 10 años la hipotermia implica una temperatura menor a 35° y a menor edad la hipotermia se va presentando con mayor temperatura; el neonato se considerara hipotérmico si tiene una temperatura menor a 37°. En pacientes politraumatizados la hipotermia tiene diferentes etiologías, y la reanimación hídrica puede generar pérdida de calor que es proporcional a la masa de líquidos administrados y al gradiente de temperatura de líquido en el paciente. La hipotermia afecta a todos los sistemas del cuerpo, los efectos adversos incluye arritmias, disminución del gasto cardíaco y de la frecuencia cardiaca, incremento de la resistencia vascular, disminución de la tasa de filtración glomerular y de la absorción de sodio, depresión del sistema nervioso central etc. Los pacientes lactantes y los recién nacidos se transfieren a una fuente de calor lo antes posible para facilitar la medición de la temperatura corporal(21).
D. Déficit neurológico (disability)/destroxtix (glicemia)/lesión de cráneo (head and eye injury) dolor
En esta sección se evalúan las cuatro “D”:
- Déficit neurológico (Disability). El traumatismo craneoencefálico causa daño nervioso primario e irreversible como resultado directo del impacto. Sin embargo, es fundamental evitar lesión secundaria debida a hipovolemia, hipotensión, hipoxia e hipercapnia.
Las evaluaciones estándar son:- Evaluación de las pupilas mediante la respuesta de la pupila a la luz (tamaño, capacidad de respuesta y simetría), es un indicador de la función troncoencefálica.
- La escala de respuesta pediátrica AVDI (alerta, verbal, dolor, inconsciente)(21,22) permite evaluar la función de la corteza cerebral y por último
- La escala de Glasgow (apertura ocular, respuesta verbal y respuesta motora).determina el nivel de conciencia y el estado neurólogo del paciente pediátrico. Si el paciente tiene una puntuación < 8 deberá ser intubado.
- Anisocoria
- Bradicardia/taquicardia
- Hipertensión
- Hiporreactividad pupilar
- Posición de descerebración o decorticación
- Descenso rápido del Glasgow Si existen, se realizará tratamiento empírico de la hipertensión con suero salino hipertónico al 3% (5 a 10 cc/kg).
Se debe buscar signos de hipertensión intracraneal:
- Glicemia (Destroxtix): Si el paciente presenta hipoglicemia se deberá pasar de forma inmediata un bolo de solución glucosada al 10% a 2 cc kg dosis.
- Déficit ocular: Lesiones oculares, de ser necesario cubrirlas con apósitos y esperar al lavado ocular en la segunda evaluación.
- Dolor: El manejo del dolor es muy importante debido a sus efectos deletéreos como consumo de oxígeno, energía, glucosa y aumento de la presión intracraneal. Por tanto, es necesario controlar el dolor lo antes posible.
El paso final de la evaluación primaria es prepararse para la segunda evaluación:
El paciente debe ser expuesto, se le quitará la ropa por completo. Una vez desnudo, se realiza una exploración rápida para localizar lesiones que no pueden esperar a ser diagnosticadas en una segunda exploración, como amputaciones, deformaciones, fracturas expuestas o lesiones en órganos internos. La inspección del paciente debe ser total, (anterior y posterior), se deben tomar las medidas de seguridad necesarias al momento de movilizar al paciente para evitar lesiones(21).
F. FAST, Fármacos y familia
El nombre de ultrasonido FAST proviene del acrónimo en inglés de Focused Abdominal Sonography for Trauma, se utiliza en Estados Unidos desde 1990 y su principal objetivo es detectar líquido libre en la cavidad abdominal de pacientes con traumatismos abdominales cerrados(23). Se valoran seis zonas:
- Espacio hepatorrenal o de Morrison
- Espacio esplenorrenal
- Correderas parietocólicas bilaterales
- Pelvis
- Pericardio
- Algunos centros valoran el tórax en busca de derrame pleural o neumotórax Las indicaciones para los exámenes de FAST incluyen: Traumatismo abdominal y/o torácico contundente y/o penetrante, shock indiferenciado y/o hipotensión (como parte del examen Rapid Ultrasound for Shock and Hypotension (RUSH)).
Este estudio, de estar disponible, se realiza en la evaluación primaria y en la sala de shock trauma.
En esta fase también se inicia la administración temprana de fármacos coadyuvantes como ácido tranexámico, analgésicos y, si es necesario, antibióticos, componentes sanguíneos, etc.
El manejo del dolor y la ansiedad en pacientes pediátricos politraumatizados es muy importante para reducir la morbimortalidad. Se inicia con ketorolaco, ketamina, fentanilo o buprenorfina según el tipo de lesión y la principal condición clínica hemodinámica y neurológica.
Solo en caso de ser necesario se deberá iniciar antibiótico de primera línea ya que una de las causas de muerte en terapia intensiva es la sepsis. Sin embargo, el inicio de antibióticos no está indicado en lesión traumática como quemaduras si no se dispone de datos clínicos o de laboratorio que sugieran la presencia de un proceso infeccioso.
FAMILIA
Este estudio, de estar disponible, se realiza en la evaluación primaria y en la sala de shock trauma.
En esta fase también se inicia la administración temprana de fármacos coadyuvantes como ácido tranexámico, analgésicos y, si es necesario, antibióticos, componentes sanguíneos, etc.
El manejo del dolor y la ansiedad en pacientes pediátricos politraumatizados es muy importante para reducir la morbimortalidad. Se inicia con ketorolaco, ketamina, fentanilo o buprenorfina según el tipo de lesión y la principal condición clínica hemodinámica y neurológica.
Solo en caso de ser necesario se deberá iniciar antibiótico de primera línea ya que una de las causas de muerte en terapia intensiva es la sepsis. Sin embargo, el inicio de antibióticos no está indicado en lesión traumática como quemaduras si no se dispone de datos clínicos o de laboratorio que sugieran la presencia de un proceso infeccioso.
Evaluación secundaria
La evaluación secundaria sólo se inicia una vez que se haya completado la evaluación primaria y se hayan tratado las lesiones que puedan poner en peligro la vida. Si durante el examen se detecta algún deterioro, se debe volver atrás a revisar la evaluación primaria.
Se debe realizar una historia clínica y exploración física detallada, estudios radiográficos y la identificación del problema, es decir de las lesiones significativas. A lo largo de la evaluación, deben observarse precauciones estándar para las infecciones transmitidas por sangre o líquidos.
Se podrá realizar la metodología MEASIRT para recordar fácilmente los pasos a seguir(18,19).
- Monitorización Mientras el líder del equipo realiza la evaluación primaria se deberá realizar la monitorización del paciente, ya que esta da una noción rápida de la respuesta al tratamiento administrado.
- Exploración céfalo caudal
- Cabeza y cara. El examen de la cabeza permite revelar un hematoma en el cuero cabelludo, una depresión o un desgarro en el cráneo. Las laceraciones del cuero cabelludo y segmentos óseos solo pueden identificarse mediante una palpación cuidadosa, por lo que la palpación del cuero cabelludo es importante, así como evaluar todas las expresiones faciales, incluida la órbita, la mandíbula superior e inferior y la nariz.
- Cuello. Se debe examinar, palpar e inmovilizarse cuidadosamente. Una mala fijación aumenta la morbilidad. Se debe suponer de una lesión en la columna cervical hasta que se demuestre lo contrario, se estudiará con imágenes radiografías o de tomografías computarizadas. Se busca dolor hinchazón y dolor agudo en la garganta.
- Tórax. Las lesiones en tórax en orden de frecuencia en el paciente pediátrico son las contusiones pulmonares, fracturas de las costillas, neumotórax y hemotórax. Se deben identificar y tratarse de emergencia en la evaluación primaria el hemotórax masivo, neumotórax a tensión y taponamiento cardiaco. El derrame pleural por neumotórax a tensión y parálisis cardíaca debe detectarse y tratarse con urgencia durante la evaluación inicial. Se debe palpar toda la pared torácica para detectar crepitación (enfisema subcutáneo) y sensibilidad. El área sobre el esternón y las clavículas requieren atención especial ya que las fracturas que afectan a estos huesos pueden sugerir una fuerza significativa y la necesidad de evaluación buscando lesiones intratorácicas. Evalúe presencia de esfuerzo respiratorio, sonidos respiratorios y cardíacos anormales. Inspeccione si hay algún hematoma relacionado con un cinturón de seguridad. Se debe tomar una radiografía de tórax y ante presencia de derrame pleural o neumotórax se debe el drenaje correspondiente.
- Abdomen. Se debe buscar signos sutiles de traumatismo abdominal cerrado por lesión de víscera maciza o hueca, estos signos son más frecuentes en el paciente inconsciente y se debe considerar que su ausencia no descarta la posibilidad de una lesión abdominal grave.
- Pelvis, periné y recto. El perineo debe ser inspeccionado para detectar cualquier evidencia de lesión. Si la sangre está presente en el meato, se debe sospechar de lesión uretral. El pubis y las espinas ilíacas anteriores deben evaluarse para detectar cualquier signo de inestabilidad pélvica. La presencia de equimosis sobre las alas ilíacas, pubis, labios o escroto y la sensibilidad a lo largo del anillo pélvico también requiere una evaluación diagnóstica. La exploración de pelvis es importante para buscar la posibilidad de fractura.
- Miembros. Las extremidades deberán evaluarse para valorar contusiones, sangrados, crepitantes, deformaciones, heridas, etc. Se deberá evaluar la integridad de las articulaciones no lesionadas por los movimientos activos y pasivos.
- Espalda. Se debe movilizar en bloque al paciente para buscar lesiones de espalda y columna vertebral. Si aún no se ha descartado lesiones en cuello debe estar inmovilizado.
- Exploración neurológica completa. La exploración neurológica será evaluada de manera completa reevaluando la exploración inicial:
- Nivel de conciencia
- Pupilas
- Escala de Glasgow
- Pares craneales
- Movilidad y tono muscular
- Sensibilidad
- Reflejos osteotendinosos
- (Historia clínica enfocada) /Documentación del cuidado En la historia clínica se debe considerar la probabilidad de maltrato y el mecanismo del trauma siempre y cuando sean conocidos. El empleo de la nemotecnia SAMPLE (signos/síntomas, alergias, medicación, historia clínica previa, ingesta última de líquidos o comida y eventos que llevaron a la enfermedad actual), servirá para poder identificar antecedentes y molestias que presenta el niño. Esta información será útil en la determinación del deterioro de la función respiratoria, neurológica o cardiovascular(21,22).
- Interconsulta Tomando en cuenta los hallazgos encontrados tanto en el primer como en la segunda evaluación física se deberá valorar las interconsultas a los diversos interconsultantes (cirujanos pediatrías, neurocirujanos, ortopedia, terapia intensiva, cirujano plástico, etc.). Por lo tanto, la decisión de trasladar un paciente politraumatizado después de la estabilización va depender de la disponibilidad de estos recursos(21,22).
- Revaloración periódica/rayos x/tomografía Durante la fase de tratamiento y estabilización, es necesario que el paciente continúe con monitorización indicada en la exploración inicial; sin embargo, se deberá prestar atención a una revaluación reiterada del paciente. El politraumatizado pediátrico puede evolucionar de una forma rápida por lo que es importante la revaloración periódica para detectar de forma oportuna cualquier complicación que se presente(24). Una vez estabilizado el paciente, se puede realizar pruebas diagnósticas específicas toma de imágenes, rayos x / tomografía (Evaluación terciaria).
- Traslado Una vez que se ha logrado la estabilización inicial de un paciente de trauma múltiple, se debe considerar solicitar al hospital de trauma que comience el tratamiento de la lesión en el primera Fase (quirúrgica). Se deberá valorar el hospital adecuado. Principalmente en nuestro medio será un hospital de tercer nivel o un centro hospitalario con experiencia en manejo de paciente politraumatizado pediátrico. Cuando se realice este traslado será cuando el paciente se encuentre lo más estable posible y haber sido aceptado por el centro hospitalario receptor. Se requiere una comunicación bidireccional entre el hospital de envío, la parte receptora y el equipo de transporte(24,25).
CONCLUSIONES
El politraumatismo se caracteriza por la presencia de múltiples lesiones y/o lesión única que pone en peligro la vida, siendo causa de muerte en el momento del accidente o en un 30% de pacientes en horas posteriores, por las complicaciones causadas por hemorragia, hipovolemia e hipoxia. El abordaje en estos pacientes requiere dirigir la atención al restablecimiento temprano de las funciones vitales del niño realizando procedimientos encaminados a evitar el daño por coagulopatias, acidosis, hipotermia, hiperglicemia e hipoxia, esto se realiza mediante el concepto de reanimación abreviada o reanimación de control de daños. Para realizar la evaluación general y el abordaje clínico, se recomienda el esquema de atención con una evaluación general que incluya el Triángulo de Evaluación Pediátrica para una evaluación diagnóstica, rápida y breve, basada en pautas visuales y auditivas del paciente, la Evaluación Primaria por medio del sistema MARCHDF, para la evaluación y tratamiento de hemorragias, vía aérea, respiración, circulación, hipotermia, déficit neurológico, lesión craneal, glucometría, exposición y ultrasonido FAST y administración de medicamentos coadyuvantes en el tratamiento (control de hemorragia, analgesia). Posteriormente se realiza la Evaluación Secundaria por medio del sistema MESIRT que permite realizar una valoración y exploración completa del paciente de cabeza a pies realizando monitorización y exploración céfalo-caudal, para ello se realiza una historia clínica dirigida por medio de la nemotecnia SAMPLE (signos/síntomas, alergias, medicación previa, historia clínica patológica previa, alimentos/líquidos y última comida, y origen de los eventos), se realizan interconsultas para abordaje multidisciplinario. Se debe realizar una revaloración periódica, con estudios de gabinete y concluir con el movimiento del paciente al centro de trauma adecuado para iniciar control de daños de fase 1 que corresponde al centro con mayor experiencia en el manejo del paciente politraumatizado pediátrico. Los procedimientos desde el manejo prehospitalario hasta el tratamiento en última instancia, requieren de una comunicación efectiva, fluida, bidireccional y de un seguimiento multidisciplinario (Figura 1).
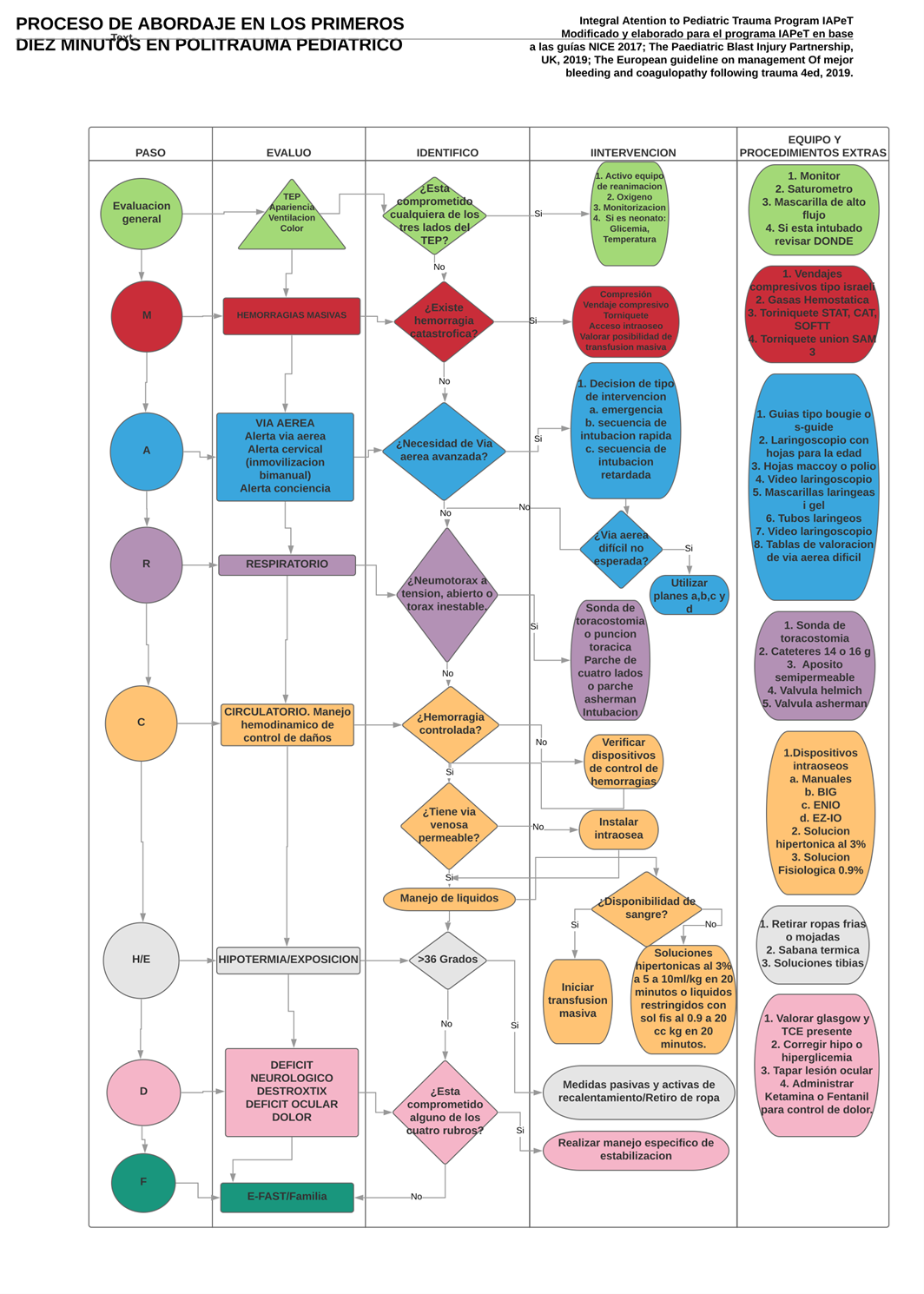
Figura 4. Protocolo MARCH-D. En donde se visualiza la fase, los datos clínicos a valorar y su abordaje terapéutico en orden de prioridad. Este protocolo está orientado al control de daños ocasionado por la triada mortal del trauma antes de la realización de cirugía de control de daños y su ingreso a esta sea lo más estable.
Contribuciones de Autoría: Los autores participaron en la concepción y diseño del artículo, recolección, análisis e interpretación de la información; revisión crítica y redacción de la versión final.
Financiamiento: Autofinanciado.
Conflictos de intereses: Los autores declaran no tener conflictos de interés en la publicación de este artículo.
Recibido: 02 de mayo 2021.
Aprobado: 14 de junio 2021.
Correspondencia: Augusto Flavio Figueroa Uribe.
Dirección: Hospital Pediátrico Peralvillo SSCDMX, Calz San Simon 14, San Simón Tolnahuac, Cuauhtémoc, 06920 Tolnahuac, CDMX – México.
Teléfono: 555 427 275 164
Correo: mandolarian1975@gmail.com
REFERENCIAS BIBLIOGRAFICAS