1. INTRODUCCIÓN
La radioterapia es una modalidad terapéutica que tiene como objetivo controlar o erradicar el volumen de tumores malignos mientras se preservan, en la medida de las posibilidades, las células sanas adyacentes a la zona tratada
1
,
2
. Esta terapia puede realizarse mediante dos técnicas distintas, dependiendo de la posición de la fuente de radiación: si el equipo que emite radiación está alejado del paciente, se denomina teleterapia; sin embargo, si la terapia se realiza utilizando radionúclidos, que se colocan cerca o están en contacto con la región tumoral, se denomina braquiterapia
3
,
4
. En ambas modalidades de tratamiento, es importante garantizar la igualdad entre la dosis prescrita y la dosis administrada al paciente, lo que resalta la importancia de la dosimetría
5
,
6
,
7
,
8
.
La dosimetría en teleterapia está guiada por el TRS-398
9
, desarrollado por el Organismo Internacional de Energía Atómica (OIEA). En contraste, la dosimetría en braquiterapia se rige por el protocolo TG-43
10
, que fue revisado posteriormente como TG-43U1
11
, establecido por la Asociación Americana de Físicos en Medicina (AAPM, por sus siglas en inglés). Este formalismo recomienda el uso de simulación de Monte Carlo debido al alto gradiente de dosis en las regiones cercanas a la fuente de braquiterapia, lo que hace que la dosimetría experimental sea altamente compleja.
Por lo tanto, se pueden usar diferentes códigos de simulación de Monte Carlo para determinar los parámetros dosimétricos responsables de esta dosimetría, entre ellos: Geant4 Application for Tomographic Emission (GATE)
12
,
13
, Monte Carlo Neutron-Photon (MCNP)
14
,
15
,PENetration and Energy LOss of Positrons and Electrons (PENELOPE)
16
,
17
y TOol for PArticle Simulation (TOPAS)
18
. La precisión de los resultados de cada código está directamente relacionada con la exactitud del transporte interno de partículas, la interacción de la radiación con la materia, así como los valores asignados por el usuario
19
.
En consecuencia, este estudio tuvo como objetivo analizar la respuesta de dos paquetes de simulación de Monte Carlo: PENELOPE y TOPAS. La validación de los simuladores se realizó para los dos escenarios de la radioterapia. Para la teleterapia, se evaluaron las dosis en profundidad porcentual utilizando haces de electrones y fotones con ambos paquetes de simulación. Para el escenario de braquiterapia, utilizando la fuente modelo IR06-103Pd de Paladio-103, se observó el comportamiento de la dosis relativa en profundidad para ambos códigos computacionales. La literatura incluye análisis dosimétricos de braquiterapia realizados en tres materiales: agua líquida, agua sólida y perspex
10
,
20
,
21
. Por lo tanto, este estudio propuso analizar la deposición de dosis para ambos escenarios de radioterapia, investigando la importancia del material que compone el fantoma, variando entre agua líquida, agua sólida y perspex.
2. MÉTODOS
2.1 Diseño
El estudio empleó un diseño comparativo entre los resultados de simulación de Monte Carlo y los valores experimentales y de la literatura. El análisis de este estudio original se basó en enfoques cuantitativos de los datos de deposición de dosis para cada uno de los escenarios de dosis tratados.
2.2 Paquete PENELOPE
El paquete de simulación PENELOPE se ejecuta en subrutinas FORTRAN y simula el transporte de electrones, positrones y fotones. Además, tiene un rango de energía disponible que va desde 1 keV hasta aproximadamente 1 GeV
22
. El método de Monte Carlo implementado en este algoritmo permite la visualización bidimensional de todas las geometrías definidas. La versión utilizada fue la 2014, y todas las simulaciones se realizaron en el clúster del Centro de Tecnología e Información de Ribeirão Preto (Ceti-RP) de la Universidad de São Paulo. Cada núcleo tiene 16 gigabytes de memoria por nodo y un procesador Intel i7.
En este código, el transporte de fotones ocurre secuencialmente, simulando interacciones una tras otra. Estos eventos están controlados por cuatro parámetros definidos por el usuario: C1, que corresponde a la desviación angular promedio producida por una colisión fuerte, lo que resulta en pérdida de energía o cambio en la dirección de la partícula, y, en consecuencia, en mayores costos computacionales; C2, que representa el valor de la pérdida de energía fraccional máxima disipada en una colisión fuerte; WCC, que simboliza la energía máxima perdida en colisiones fuertes; y finalmente, WCR, que es la energía máxima perdida por una partícula cargada en emisiones significativas de radiación de frenado
22
,
23
.
2.3 Paquete de simulación TOPAS
El paquete de simulación TOPAS opera utilizando la herramienta del algoritmo GEANT4 del código de simulación de Monte Carlo. Fue desarrollado con una interfaz más intuitiva, lo que permite la visualización tridimensional de las geometrías. Este código permite la simulación de protones
24
, además de las partículas que también son transportadas por PENELOPE. TOPAS fue desarrollado para la física de altas energías, alcanzando niveles radiobiológicos y clínicos
18
, variando así su rango de energía disponible desde 1 eV hasta valores cercanos a TeV. La versión utilizada fue la 3.5, y todas las simulaciones se realizaron en una computadora personal. Para este código, se cargó la lista de recursos de física de PENELOPE incrustada en GEANT4.
2.4 Escenarios de simulación
Las simulaciones se modelaron utilizando un fantoma cúbico de simulación con lados de 30 cm, dividido en 101 píxeles en cada una de las tres direcciones del eje cartesiano. El relleno de este fantoma varió entre tres materiales diferentes: agua líquida, agua sólida y perspex. La composición de los dos últimos materiales se configuró según Rodríguez et al., en 2005, y Saidi et al., en 2011
20
,
21
. respectivamente. Las fracciones de peso (W) y densidades (ρ) se enumeran en la tabla 1. El número de partículas primarias simuladas se mantuvo constante en 5x108.
Tabla 1. Fracciones de peso de cada constituyente y densidades de los materiales del fantoma.
| Material |
W H |
W ° |
W c |
W N |
W Ca |
W Cl |
ρ(g/cm3) |
| Agua líquida |
66,00% |
34,00% |
- |
- |
- |
- |
01,00 |
| Agua sólida* |
08,09% |
19,84% |
67,22% |
02,40% |
02,32% |
00,13% |
01,01 |
| Perspex** |
08,00% |
32,00% |
60,00% |
- |
- |
- |
01,19 |
*Rodríguez et al., en 2005
20
; ** Saidi et al., en 2011
21
.
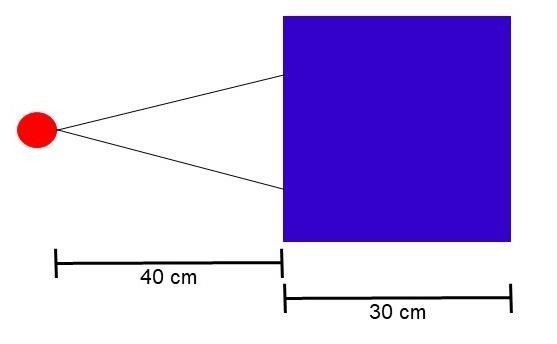
En el escenario de la teleterapia, la fuente se posicionó a 40 cm de la superficie del fantoma, con un campo de irradiación cuadrado de 5 cm por lado. El esquema de irradiación se muestra en la Figura 1a. Se analizaron haces de fotones y electrones, ambos de 6 MeV. Los valores de los parámetros de condensación (C1 y C2) se establecieron en 0.1; WCC y WCR se definieron como 1x103 y 1x104, respectivamente, y la energía de absorción para electrones, fotones y positrones (EABS) se fijó en 1x104 eV y 2x105 eV.
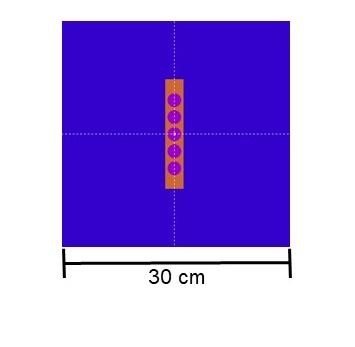
En el escenario de la braquiterapia, la fuente simulada fue Paladio-103, modelo IR06-103Pd, según Saidi & Sadeghi (2019)
25
y se modeló en el centro del fantoma, como se muestra en la Figura 1b. Estas simulaciones utilizaron las 8 líneas principales de emisión de fotones, que van desde 20.07 keV hasta 497.1 keV. Los valores de C1 y C2 se fijaron en 0.3 para optimizar el tiempo de simulación, mientras que WCC y WCR se definieron como 5x10 3, y EABS se estableció en 5 keV.
Figura 1
Escenarios de simulación: a) teleterapia, b) braquiterapia
a)
b)
3. RESULTADOS Y DISCUSIÓN
En el presente estudio, se analizaron dos escenarios de tratamiento de radiación, teleterapia y braquiterapia, mediante simulación. Para el primero, se evaluó la dosis en profundidad porcentual, mientras que, para el segundo, se observó la dosis relativa.
3.1 Escenario de teleterapia
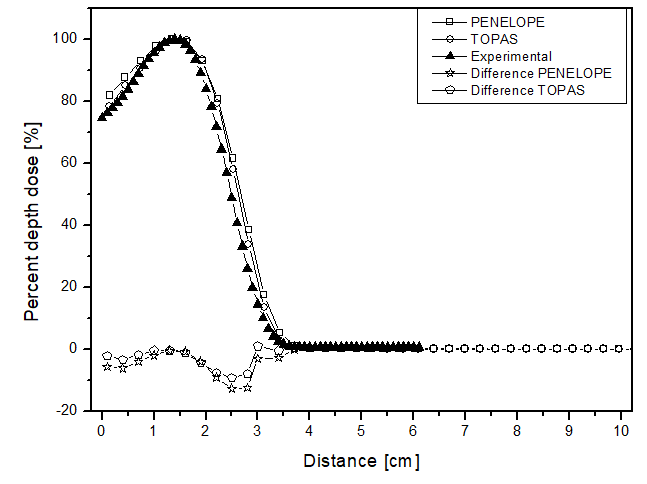
El escenario permitió el análisis de dos haces diferentes. Las Figuras 2 y 3 presentan el comportamiento de los haces de electrones y fotones, respectivamente. Al analizar los gráficos en la figura 2, se observa una fuerte disminución en el rendimiento hasta aproximadamente 4 cm de distancia para todos los materiales en ambos casos. El comportamiento de los simuladores se alinea con las expectativas experimentales, ya que la curva experimental de deposición de dosis en la figura 2a corresponde a las curvas simuladas. La mayor diferencia puntual entre las simulaciones en agua líquida en comparación con el experimento fue de 12 p.p con el método Monte Carlo de PENELOPE. Sin embargo, después de 5 cm de profundidad, la dosis capturada por píxel es aproximadamente cero en ambos simuladores. También se comparó la mayor variación entre las curvas de cada simulador en cada uno de los materiales que llenan el fantoma. PENELOPE mostró la mayor diferencia en comparación con TOPAS, 4 p.p, cuando se llenó con agua líquida. Entre todos los escenarios desarrollados para el haz de electrones, la incertidumbre máxima encontrada fue inferior al 4.5%.
Figura 2
Dosis en profundidad porcentual en función de la distancia para el escenario de teleterapia con electrones, con el fantoma lleno de: a) agua líquida, b) agua sólida y c) perspex
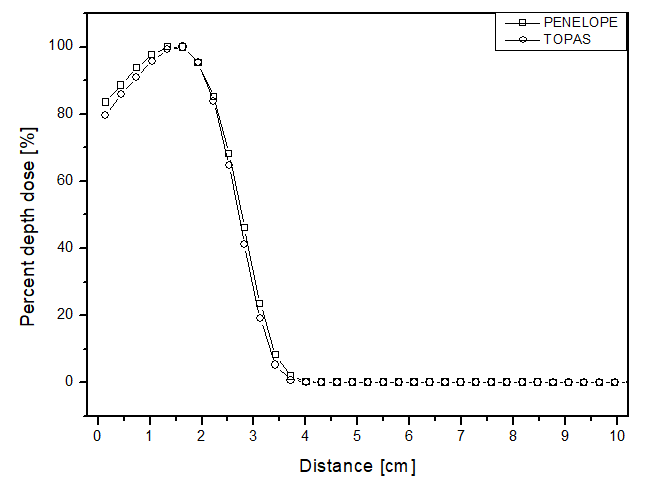
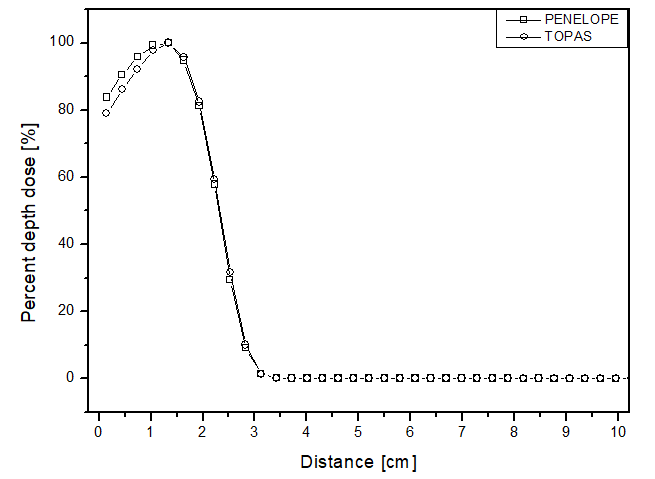
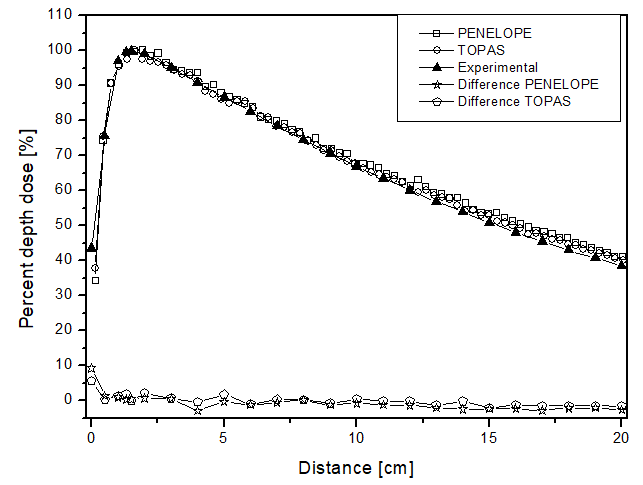
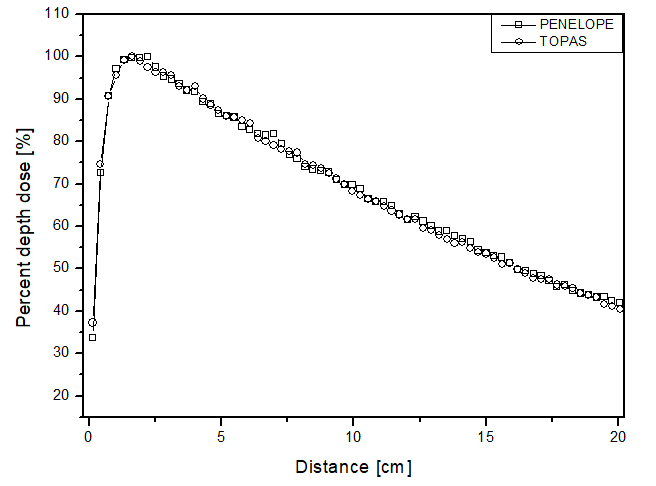
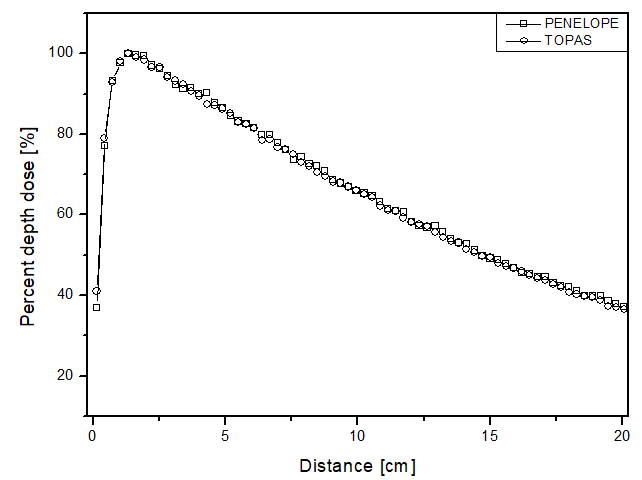
A diferencia del haz de electrones, para el haz de fotones, la dosis se encuentra a lo largo de los 10 cm de análisis. El comportamiento de las curvas es similar para ambos códigos computacionales, ya que la mayor diferencia encontrada fue de 4 p.p, que fue mayor para el paquete de simulación TOPAS cuando el fantoma se llenó con perspex. La mayor incertidumbre encontrada en las simulaciones para el haz de fotones fue de aproximadamente 4.5%. En el análisis comparativo con los datos experimentales, nuevamente, el comportamiento de la deposición de dosis de los dos simuladores pudo ser validado. Esto se debe a que la mayor diferencia encontrada fue de 9 p.p, a una distancia de 0.14 cm, siendo PENELOPE el que más se distanció de los datos experimentales. Estos datos se muestran en la figura 3a.
Figura 3
Dosis en profundidad porcentual en función de la distancia para el escenario de teleterapia con fotones y fantoma lleno de: a) agua líquida; b) agua sólida y c) perspex
3.2 Escenario de braquiterapia
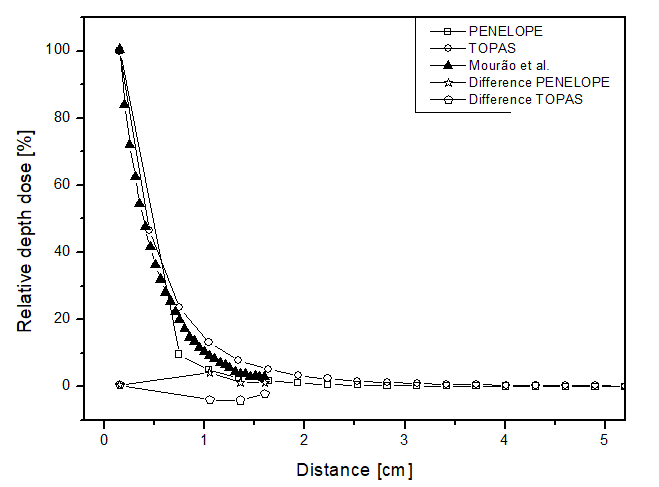
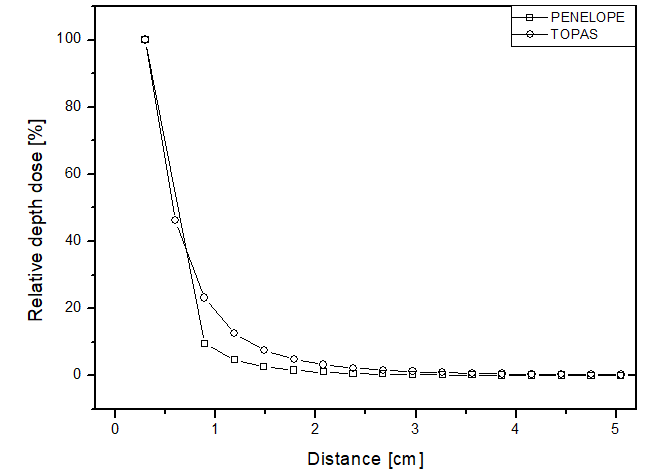
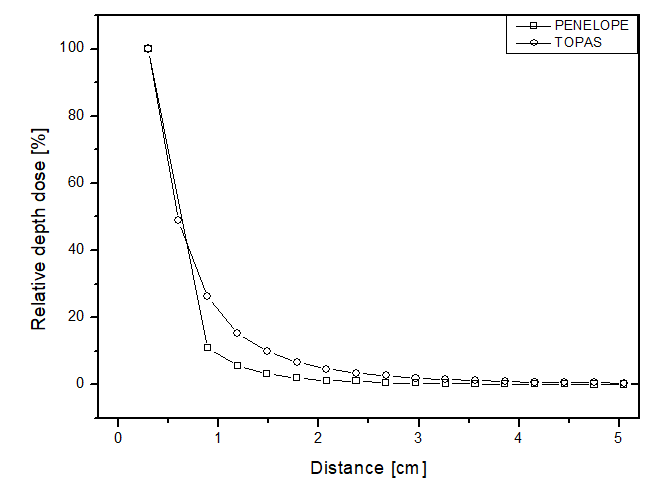
En este escenario, la comparación entre los simuladores se realizó mediante la dosis relativa a lo largo de la dirección radial desde la fuente para cada uno de los materiales. La Figura 4 presenta los resultados obtenidos, mostrando comportamientos similares entre los dos simuladores, pero la deposición de dosis puntual hasta una distancia de 2 cm varió hasta 15 p.p entre las curvas para todos los materiales. La Figura 4a muestra la curva de dosis obtenida por Mourão & Campos, en 2010
26
, donde la mayor diferencia puntual fue de aproximadamente 4 p.p para ambos simuladores. Así, como se esperaba para una fuente de radiación de braquiterapia, la deposición de dosis obtenida en las simulaciones fue rápida, siendo aproximadamente cero después de una distancia de 3 cm. Esto confirma la dificultad de realizar dosimetría de manera experimental, considerando el desafío de colocar un dosímetro a tal distancia de una fuente para garantizar una detección adecuada. Los simuladores lograron una incertidumbre relativa máxima por debajo del 5% para todos los materiales, cumpliendo así con las recomendaciones de la AAPM.
Figure 4
Percentage depth dose as a function of distance for the brachytherapy scenario, with phantom filled with: a) liquid water; b) solid water; c) perspex.
De este modo, los resultados presentados para ambos escenarios están de acuerdo con lo esperado, tanto clínicamente como en la literatura. Por lo tanto, se puede considerar que los dos métodos computacionales de Monte Carlo evaluados son herramientas prometedoras para realizar dosimetría en braquiterapia. Además, la concordancia con los resultados experimentales permite validar los códigos como instrumentos para simulaciones más avanzadas que ayuden a predecir la deposición de dosis en pacientes para nuevas técnicas de tratamiento que pueden ser estudiadas.
4. CONCLUSÓN
En el presente estudio, se analizaron los perfiles de dosis en profundidad para dos tipos de haces de teleterapia. En ambos casos, el comportamiento fue similar al que se espera en la literatura, ya que el haz de electrones mostró una caída más pronunciada que el haz de fotones. Además, el haz de electrones exhibió menor penetrabilidad a lo largo del fantoma, similar a lo que ocurre clínicamente, considerando que los haces de electrones se utilizan para tratamientos superficiales como la terapia de piel.
El escenario de braquiterapia también arrojó resultados satisfactorios para la comparación de los simuladores. Las curvas para este tipo de fuente mostraron respuestas similares, con una variación puntual de 4 p.p. cerca de 1 cm. Además, el comportamiento de las curvas es análogo a la literatura, con baja incertidumbre obtenida para ambos códigos computacionales. Por lo tanto, el análisis presentado en este estudio demuestra que los paquetes de simulación PENELOPE y TOPAS exhiben una alta concordancia en los resultados para los escenarios de teleterapia y braquiterapia.
Asimismo, los sistemas de simulación respondieron a las diferentes composiciones de los fantomas, mostrando una variación de 4 p.p. y 15 p.p. para teleterapia y braquiterapia, respectivamente. Por lo tanto, los códigos de simulación estudiados emergen como herramientas prometedoras para aplicaciones en dosimetría.
Acknowledgements
Los autores agradecen al Centro de Tecnología e Información de Ribeirão Preto (Ceti-RP) y al Profesor Alexandre Bonatto, del Grupo de Física de Haces de la Universidad Federal de Ciencias de la Salud de Porto Alegre (UFCSPA), por los recursos computacionales disponibles para realizar las simulaciones, los cuales fueron adquiridos con la ayuda del Consejo Nacional de Desarrollo Científico y Tecnológico (CNPq) (Llamada Universal 427273/2016-1 y 405143/2021-4) y la Fundación de Apoyo a la Investigación del Estado de Rio Grande do Sul (FAPERGS) (PqG 21/2551-0002027-0).